









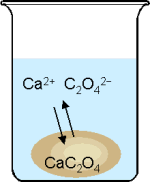
Lösungs- und Fällungsprozesse sind Gleichgewichtsreaktionen: Ca2+ + C2O42–
Gibt man ein schwerlösliches Salz in Wasser, wird sich ein wenig des Salzes lösen. Man erhält über dem festen Salz ("Bodenkörper") eine gesättigte Lösung. Die Konzentrationen der Ionen in der Lösung sind abhängig von der Art des Salzes und der Temperatur. Aus den Konzentrationen kann das Löslichkeitsprodukt Lp berechnet werden: Lp = [Ca2+] · [C2O42–] Das Löslichkeitsprodukt ist ein konstanter Wert, der für jede schwerlösliche
Verbindung charakteristisch ist. Je größer das Löslichkeitsprodukt ist, desto mehr Salz kann
gelöst werden. |
 |
| Verbindung | Löslichkeitsprodukt (Lp) | Konzentration von Ca2+ bzw. Mg2+ in der gesättigten Lösung |
| CaC2O4·H2O (Whewellit) | 1,8·10–9 mol2/l2 | 1,7 mg/l |
| CaCO3 (Calcit) | 4,8·10–9 mol2/l2 | 2,8 mg/l |
| CaHPO4·2H2O (Brushit) | 5,0·10–6 mol2/l2 | 88 mg/l |
| Ca3(PO4)2 (Apatit) | 1,0·10–25 mol5/l5 | 0,5 mg/l |
| Mg(NH4)PO4·6H2O (Struvit) | 2,5·10–13 mol3/l3 | 1,5 mg/l |


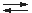 CaC2O4
¯
CaC2O4
¯